复方配伍保健食品备案,终结“单一原料内卷”,开辟产业高质量发展新赛道。
复方君臣佐使配伍保健食品终于开启备案试点。
这意味着,复方保健食品终于不用遵循“注册制”,通过备案试点即可。
目前我国保健食品备案以单一原料或简单复配为主,难以体现中医药“君臣佐使”的配伍理念,也无法满足消费者对多功能养生产品的需求。
此次试点是通过规范复方配伍保健食品的备案流程,以“备案制”替代部分“注册制”,简化创新产品上市流程,推动备案保健食品行业从“单一原料”向“复方功效协同”升级。
试点以药食同源物质为复方核心原料,本质是将中医药理论与现代保健食品结合,推动“药食同源”从“传统食材”向“功能性原料”升级。
通过“原料白名单”、“配方数量限制”、“全周期追溯”等要求,让药食同源复方产品“配方逻辑”、“安全依据”更加透明。
01
国产复方配伍保健食品备案试点可选择的原料名单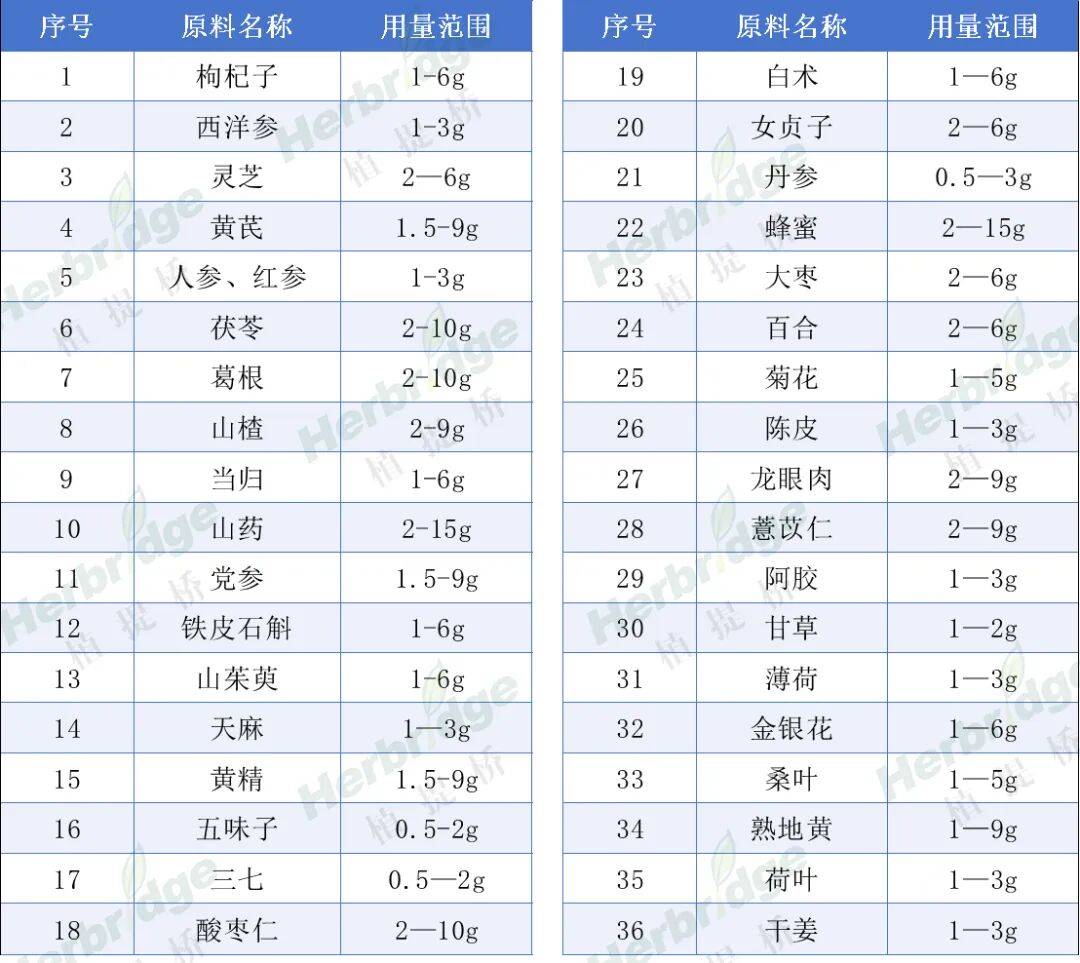
说明:
1)限数量、倡精简的配方逻辑;备案产品原料数量不超过14个,其中药食同源之外的原料,不超过4个。
2)适宜人群:
与《允许保健食品声称的保健功能目录非营养素补充剂( 2023年版》中保健功能相对应的人群;
可结合传统中医养生理论细化人群描述。
3)不适宜人群:
少年儿童、孕妇、乳母;
结合产品的特点,可细化传统中医中禁忌人群的描送。
4)注意事项:西洋参、党参、丹参不宣与含有藜芦的中草药及其制品同用。红参、人参不宜与含有藜芦、五灵脂的中草药及其制品同用。
5)试点产品可选择的功效及要求
可选择《允许保健食品声称的保健功能目录非营养素补充剂(2023年版》范围内的保健功能,以及符合我国保健食品监管定位和传统中医养生理论的保健功能。
产品备案时可选择1-2个保健功能声称。对于申报2个保健功能的,还应当提供不同保健功能可同时声称的合理性依据。
02
文件其它核心内容盘点
● 试点期限:为批复之日起3年;
● 备案人资质要求:相应的研发、生产、检验能力;
备案人应当为获得保健食品注册证书或者保健食品备案凭证并已转化实际生产的保健食品生产企业。五年内产品未出现过不合格的情形,且近三年内未受到行政处罚等。
● 功效验证:备案前完成动物实验、人体试食试验;按照《保健食品功能检验与评价技术指导原则(2023年版)》《保健食品功能检验与评价方法(2023年版)》等规定开展功能性评价试验。
● 试点产品备案号:(省)食健备(试)G+4位年代号+2位省级行政区域代码+6位顺序编号,其中顺序编号由各省(区、市)自行制定。
● 产品销售与追溯:在本省(区、市)内线下销售至保质期结束。
● 试点流程:
试点申请——技术审查——技术咨询——试点核准——信息归集——试点监管——试点取消——试点转归。
03
小结
试点对企业的研发、生产、检验能力及数据追溯提出明确要求,企业需投入资金用于人才储备、设备升级、检测及合规体系建设。
试点备案的核心参与者是那些具备研发实力、合规记录良好的头部企业,可依托现有中医药研发团队,结合“君臣佐使”理论开发差异化复方产品;借助试点备案制的便捷性,快速将创新配方转化为产品,抢占市场先机。
想要了解更多关于药食同源法规进程以及科学研究、产品创新的话题,欢迎大家参与2025年10月24-26日在南京国际展览中心(新庄)举办的第2届【药食同源|滋补品升维开发峰会】及第16届【AAES天然健康产品展& AAES天然健康产品行业大会】,届时将邀请专家(如“三新”评审专家闫文杰)及行业领袖深入探讨食药物质相关的关键议题。
大会日程:药食同源新品类、抗衰新趋势、技术新红利、洞悉产业新增长|AAES2025更新日程
合作/报名联系:

END 温馨提示: 亲爱的朋友们,公众号推送机制发生改变,进入植提桥公众号主页,设置星标,及时收获新鲜推文,与行业共同进步,不掉队。 星标指南: 文章转载,请后台回复小桥; 文章配图不涉及商业行为,如有疑问,请后台回复小桥; 本文仅代表作者本人观点,不代表植提桥立场,内容仅出于信息传播和交流目的;不代表我们绝对认同相关宣称,也不支持任何产品销售。 点赞 分享 留言



都在搜:药食同源复方产品开发要点
写留言






